GORE® VIABIL®
Endoprótesis biliar de alambre corto
Endoprótesis biliar de alambre corto
Con una tasa de migración reportada promedio del 0,25 %, estamos tan seguros de estos resultados que lo reemplazaremos si ocurre una migración.6,7
Las aletas antimigración totalmente cubiertas sujetan firmemente el dispositivo dentro del conducto para minimizar el riesgo de migración, con una tasa de migración reportada del 0,0 al 1,4 %. Esto supera las tasas de migración del stent BOSTON SCIENTIFIC WALLFLEX Biliary RX totalmente cubierto, que oscilaban entre el 0 y el 13 %. 1
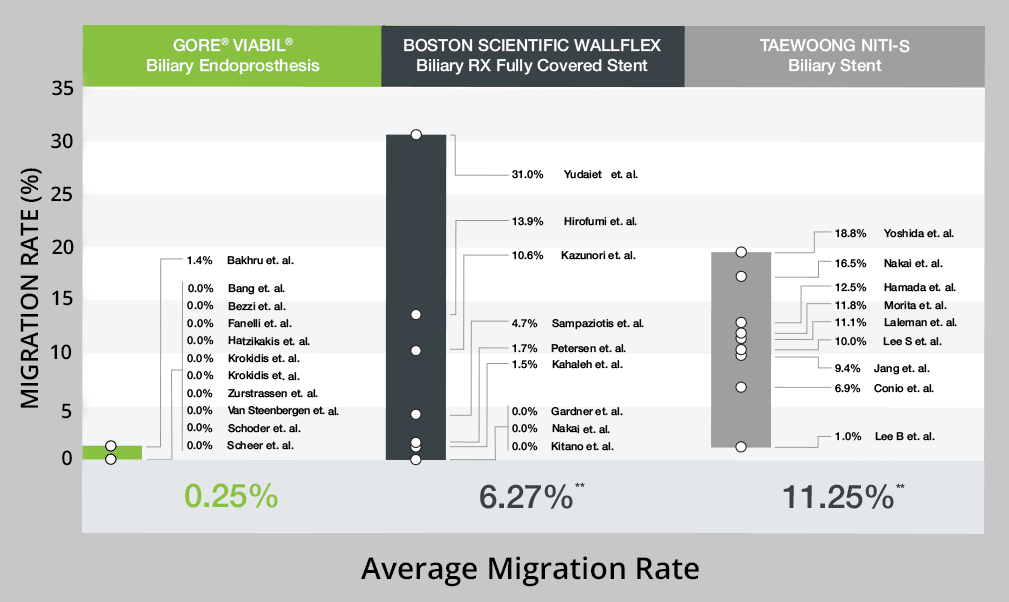
Comparación de la tasa de migración de la estenosis biliar maligna1
La endoprótesis biliar autoexpandible GORE® VIABIL® de alambre corto es el único stent metálico totalmente recubierto y sin escorzo que permanece en la misma posición durante todo el despliegue, eliminando la necesidad de usar la técnica de empuje-tracción. Los médicos pueden confiar en que la longitud y la posición del stent serán las mismas antes y después del despliegue. La combinación de un despliegue sin escorzo y tecnología antimigración ha demostrado minimizar el riesgo de reintervención.1
La permeabilidad, o la capacidad de un stent de permanecer abierto y sin oclusiones, es una característica crucial de cualquier stent metálico autoexpandible.
La endoprótesis biliar GORE® VIABIL® mantiene una permeabilidad primaria mayor que el stent principal a los 3, 6 y 12 meses después de su implantación2,3 gracias a su fuerza radial moderada, su baja fuerza axial y su revestimiento duradero y no poroso de ePTFE/FEP. Una mejor permeabilidad a largo plazo puede mejorar la calidad de vida de los pacientes.
GORE® VIABIL® ofrece un equilibrio óptimo entre una fuerza axial (Af) baja y una fuerza radial (Rf) moderada, lo que permite una adaptación natural del stent a la anatomía del conducto biliar, manteniendo al mismo tiempo las tasas de permeabilidad primaria líderes en la industria. Un ajuste y una flexibilidad adecuados pueden ayudar a prevenir la migración y la formación de lodos.4,5
Equilibrio óptimo de fuerza: La combinación preferida de baja Af y Rf moderada para minimizar el riesgo de migración, adaptándose naturalmente a la anatomía del conducto biliar.4
Baja fuerza axial: Reduce la migración, las torceduras, la formación de lodos y la colangitis.5
“Confío en la endoprótesis biliar GORE® VIABIL®. Entre sus características más importantes se encuentran: sus propiedades antimigratorias, comprobadas; la ausencia de escorzo durante y después del despliegue; la precisión de colocación gracias a que el stent se despliega directamente desde el catéter en lugar de ser expulsado de una vaina; y su adaptabilidad al biopulmón.”


Todd Baron, MD
Gastroenterólogo y profesor de Medicina en la Facultad de Medicina de la Universidad de Carolina del Norte
* Si se despliega según las instrucciones, la endoprótesis no se acortará apreciablemente. Datos en archivo.
** p<0.00000001, when compared to GORE® VIABIL® Biliary Endoprosthesis migration rates.
1 W. L. Gore & Associates, Inc; Biliary Fully Covered Metal Stents Systematic Review of the Clinical Literature. Flagstaff, AZ; 2019. [Work plan]. WP111272.
2 Krokidis M, Fanelli F, Orgera G, Bezzi M, Passariello R, Hatzidakis A. Percutaneous treatment of malignant jaundice due to extrahepatic cholangiocarcinoma: covered Viabil stent versus uncovered Wallstents. Cardiovascular & Interventional Radiology 2010;33(1):97-106.
3 Kitano M, Yamashita Y, Tanaka K, et al. Covered self-expandable metal stents with an anti-migration system improve patency duration without increased complications compared with uncovered stents for distal biliary obstruction caused by pancreatic carcinoma: a randomized multicenter trial. Am J Gastroenterol. 2013 Nov;108(11):1713-22.
4 Isayama H, Nakai Y, Toyokawa Y, et al. Measurement of radial and axial forces of biliary self-expandable metallic stents. Gastrointestinal Endoscopy 2009;70(1):37-44.
5 Isayama H, Mukai T, Itoi T, et al. Comparison of partially covered nitinol stents with partially covered stainless stents as a historical control in a multicenter study of distal malignant biliary obstruction: the WATCH study. Gastrointestinal Endoscopy 2012;76(1):84-92.
6 W. L. Gore & Associates, Inc; Radial Force and Bend Stiffness Characterization of Biliary Stents. Flagstaff, AZ; 2012. [Work plan]. WP103837.
8 Sujeto a términos y condiciones, MCM2017139
9 W. L. Gore & Associates, Inc. Reducir el riesgo de reintervención. GORE® VIABIL® Biliary Endoprosthesis Assurance Brochure. Flagstaff, AZ: W. L. Gore & Associates, Inc.
| CAT # | VSWVN0804 |
| Diameter | 8mm |
| Length | 40mm |
| Working Length of Delivery Catheter | 200cm |
| CAT # | VSWVN0806 |
| Diameter | 8mm |
| Length | 60mm |
| Working Length of Delivery Catheter | 200cm |
| CAT # | VSWVN0808 |
| Diameter | 8mm |
| Length | 80mm |
| Working Length of Delivery Catheter | 200cm |
| CAT # | VSWVN0810 |
| Diameter | 8mm |
| Length | 100mm |
| Working Length of Delivery Catheter | 200cm |
| CAT # | VSWVN1004 |
| Diameter | 10mm |
| Length | 40mm |
| Working Length of Delivery Catheter | 200cm |
| CAT # | VSWVN1006 |
| Diameter | 10mm |
| Length | 60mm |
| Working Length of Delivery Catheter | 200cm |
| CAT # | VSWVN1008 |
| Diameter | 10mm |
| Length | 80mm |
| Working Length of Delivery Catheter | 200cm |
| CAT # | VSWVN1010 |
| Diameter | 10mm |
| Length | 100mm |
| Working Length of Delivery Catheter | 200cm |
| CAT # | VSWVH0806 |
| Diameter | 8mm |
| Length | 60mm |
| Working Length of Delivery Catheter | 200cm |
| Transmural Drainage Holes Length | 2cm |
| CAT # | VSWVH0808 |
| Diameter | 8mm |
| Length | 80mm |
| Working Length of Delivery Catheter | 200cm |
| Transmural Drainage Holes Length | 2cm |
| CAT # | VSWVH0810 |
| Diameter | 8mm |
| Length | 100mm |
| Working Length of Delivery Catheter | 200cm |
| Transmural Drainage Holes Length | 2cm |
| CAT # | VSWVH1006 |
| Diameter | 10mm |
| Length | 60mm |
| Working Length of Delivery Catheter | 200cm |
| Transmural Drainage Holes Length | 2cm |
| CAT # | VSWVH1008 |
| Diameter | 10mm |
| Length | 80mm |
| Working Length of Delivery Catheter | 200cm |
| Transmural Drainage Holes Length | 2cm |
| CAT # | VSWVH1010 |
| Diameter | 10mm |
| Length | 100mm |
| Working Length of Delivery Catheter | 200cm |
| Transmural Drainage Holes Length | 2cm |